SMQ ISO 13485 structuré et évolutif pour dispositifs médicaux et IVD
ReadySet propose un SMQ ISO 13485 structuré, organisé en espaces dédiés dans Confluence pour faciliter la gestion de votre système qualité.
Cette architecture permet de distinguer clairement les processus, les enregistrements et la documentation technique, tout en assurant une traçabilité complète à l’échelle du système.
Espace SMQ ISO 13485 – Processus opérationnels
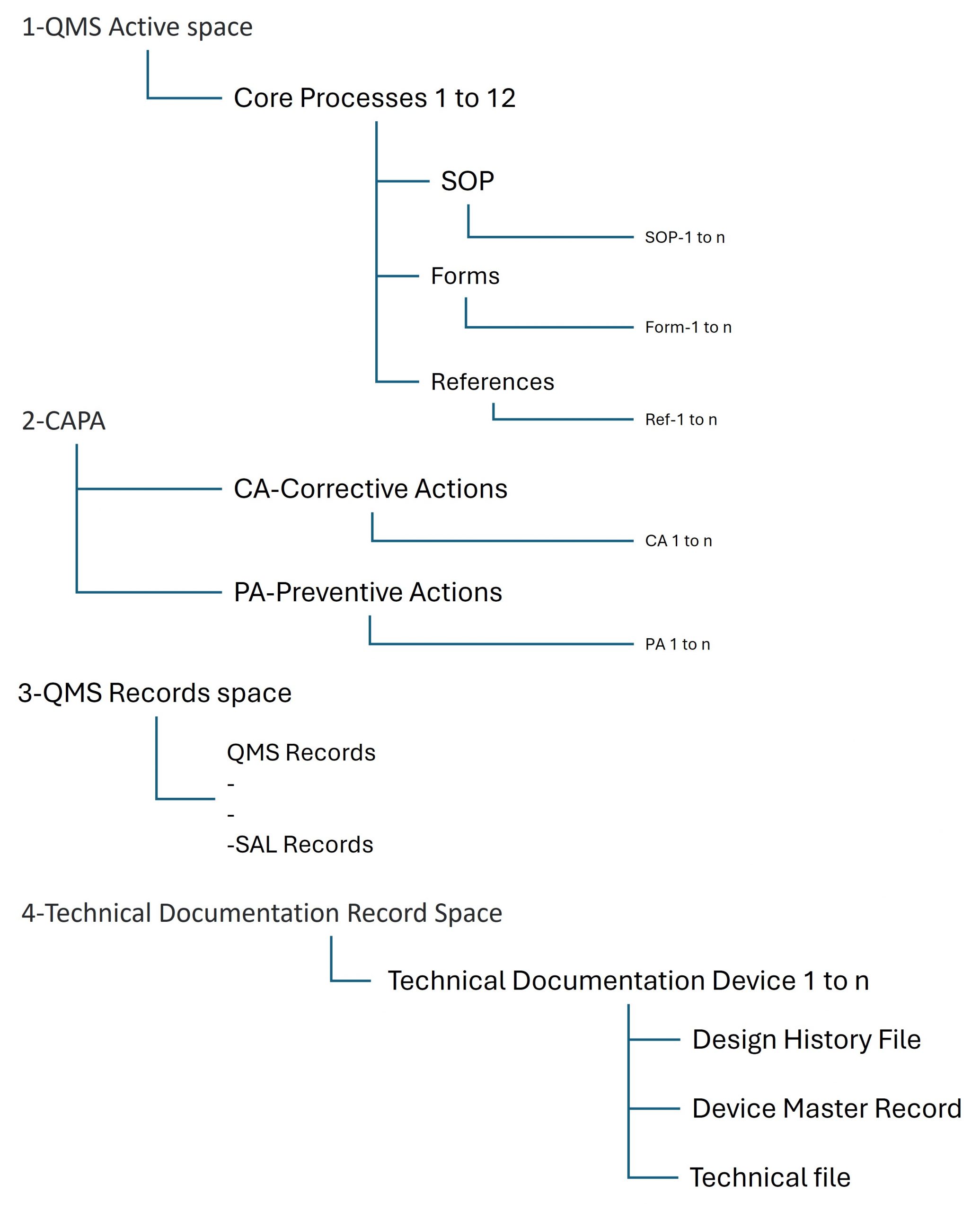
L’espace QMS Active contient la structure opérationnelle du système qualité.
Il regroupe les processus nécessaires au fonctionnement d’un QMS conforme à ISO 13485, organisés autour des 12 processus cœur présentés dans votre documentation actuelle.
Chaque processus comprend trois grands types de documents contrôlés :
• SOP pour décrire les processus
• Forms pour collecter les données et générer les enregistrements qualité
• References pour les références internes et réglementaires
L’analyse de risque est également gérée dans le QMS Active Space au moyen de formulaires dédiés.
Cela permet d’intégrer les activités d’analyse de risque directement au fonctionnement du SMQ, avec des données structurées, des évaluations traçables et des liens avec les processus concernés.
Cette approche rend le système plus pratique, plus cohérent et plus facile à auditer.
Gestion CAPA dans un SMQ ISO 13485
ReadySet comprend un espace CAPA dédié à la gestion des actions correctives et préventives.
Cette structure couvre l’ensemble du cycle CAPA :
• identification des problèmes
• investigation et analyse des causes
• actions correctives
• actions préventives
• suivi et vérification d’efficacité
Gestion des enregistrements du SMQ ISO 13485
L’espace QMS Records stocke les enregistrements générés lors de l’exécution des processus et de l’utilisation des formulaires.
Ces enregistrements constituent les preuves objectives de la bonne application du système qualité.
Les documents types peuvent inclure :
- dossiers de formation
- dossiers fournisseurs
- comptes rendus de revues de direction
- dossiers opérationnels et qualité
Cet espace dédié permet de maintenir une séparation claire entre les procédures en cours et les documents conservés.
Documentation technique dans un SMQ ISO 13485
ReadySet comprend également un espace dédié à la documentation technique pour un ou plusieurs dispositifs.
Pour chaque dispositif, la structure peut inclure :
• Design History File (DHF)
• Device Master Record (DMR)
• Technical File
Cela permet de séparer la documentation produit du système de gestion de la qualité (SGQ) central tout en préservant la cohérence et la traçabilité de l’ensemble du système.
Illustration de l’architecture ReadySet
Cette vidéo détaillée explique l’architecture de ReadySet et montre comment déployer et utiliser le framework dans Confluence.
Pourquoi ce SMQ ISO 13485 est efficace
Cette architecture apporte plusieurs avantages :
• séparation claire entre procédures, enregistrements et documentation technique
• analyse de risque intégrée au QMS opérationnel
• gestion documentaire plus simple
• meilleure traçabilité
• préparation plus rapide aux audits
• évolutivité avec la croissance de l’entreprise
Le résultat est un système qualité réellement opérationnel, et pas uniquement un ensemble de documents.
